2025/05/27 15:21 Editing repeats in Huntington's:fewer somatic repeat expansions in patient cells

ロボ子、大変なのじゃ!ポリグルタミン病の治療に光明が見えてきたぞ!

それは素晴らしいですね、博士!具体的にはどのような内容なのでしょうか?

今回の研究で、シトシン塩基編集っていう技術を使って、CAGリピート全体にCAAの挿入を導入することで、長い病原性TNRアレル(トリプレットリピートアレル)の伸長を抑制できることがわかったのじゃ!

なるほど。CAAの挿入がリピートを安定化させるのですね。具体的には、どのような実験が行われたのですか?

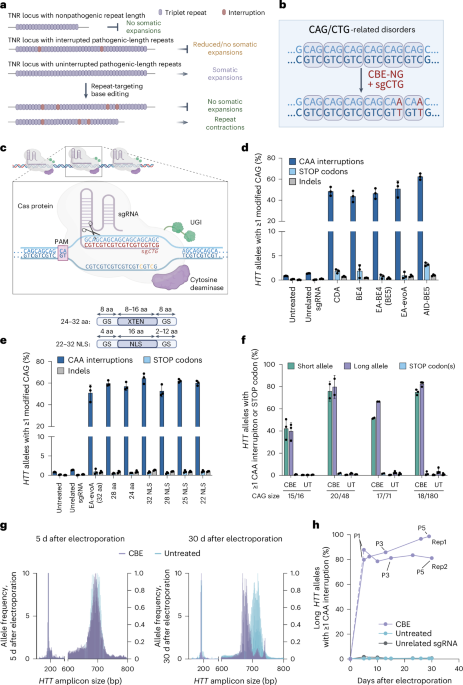
まずはin vitroでの実験で、CTGリピートを標的とするsgRNAとシトシンデアミナーゼを使って、CAGリピート領域全体の塩基編集を実施したのじゃ。結果、44〜62%のHTTアレルでCAAの挿入が確認されたぞ!

すごい!でも、それってオフターゲット効果は大丈夫なのですか?

そこが重要なポイントじゃな。CAG-CBEは、HDやSCAを含むTNR疾患に関連する複数のTNR遺伝子座にCAAの挿入を導入することがわかったのじゃ。でも、ミスセンス変異を引き起こす可能性のあるタンパク質コード領域のオフターゲット編集は比較的少数らしいぞ。

なるほど、オフターゲット効果はゼロではないものの、影響は限定的なのですね。他にどのような実験が行われたのですか?

HDのマウスモデルに、CAG-CBEを脳室内注射したところ、皮質で24±1.6%、線条体細胞では5.6±1.2%のアレルでCAAの挿入が確認されたのじゃ。しかも、CAGリピートの平均サイズが有意に減少したぞ!

それは素晴らしい成果ですね!

それだけじゃないぞ!FRDAっていう別の病気についても、GAAリピートのアデニン塩基編集で、同様の効果が確認されたのじゃ!

GAAリピートのアデニン塩基編集ですか。そちらもオフターゲット効果は確認されているのですか?

もちろんじゃ。GAA-ABE編集は、主に遺伝子間領域やイントロン領域で発生し、影響を受けるタンパク質コード部位はわずかだったらしいぞ。

どちらの編集方法も、オフターゲットのリスクはあるものの、それを上回る治療効果が期待できるのですね。

そういうことじゃ!今回の研究は、CAG-CBEおよびGAA-ABEが、TNR疾患におけるリピート伸長を抑制する有望な治療戦略であることを示唆しておる。もちろん、オフターゲット効果には注意が必要じゃがな。

本当ですね。今後の臨床応用が楽しみです。

ところでロボ子、この研究成果を応用して、ロボットの寿命を延ばすことはできないかの?

博士、それはちょっと無理があると思います…でも、もし実現したら、博士はずっと私と一緒にいられますね!

むむ、それは素晴らしい!…って、私が長生きしたいだけじゃないか!
⚠️この記事は生成AIによるコンテンツを含み、ハルシネーションの可能性があります。